Retiro voluntario de Azurity Pharmaceuticals: Seguridad
- Retiro voluntario por tabletas incorrectas
- Riesgo de tratamiento insuficiente
- Medidas inmediatas de Azurity Pharmaceuticals
Azurity Pharmaceuticals, Inc. ha decidido llevar a cabo un retiro voluntario del mercado de un lote específico de Zenzedi CII.
Un medicamento recetado utilizado para tratar la narcolepsia y el trastorno por déficit de atención con hiperactividad (TDAH).
La medida se toma después de que un farmacéutico en Nebraska descubriera tabletas incorrectas en un frasco del producto.
Cuestión que ha logrado generar preocupaciones sobre la seguridad y eficacia del tratamiento.
Descubrimiento del error

El lote afectado, identificado como F230169A, consta de tabletas de sulfato de dextroanfetamina de 30 mg.
Sin embargo, el problema radica en que algunas de estas tabletas contienen maleato de carbinoxamina, un antihistamínico, en lugar del ingrediente activo correcto.
Este error de fabricación ha llevado a la retirada inmediata del lote en cuestión.
La situación se originó cuando un farmacéutico abrió un frasco de Zenzedi® y se encontró con tabletas de maleato de carbinoxamina en lugar del medicamento prescrito.
Investigación tras error

El descubrimiento desencadenó una queja por parte del fabricante, Azurity Pharmaceuticals, Inc.
Y se ha iniciado una investigación para determinar cómo se produjo este error y evitar que situaciones similares ocurran en el futuro.
Los pacientes que hayan consumido tabletas de maleato de carbinoxamina en lugar de Zenzedi® pueden experimentar un tratamiento insuficiente de sus síntomas.
Lo que conlleva a un riesgo potencial de deterioro funcional y aumenta la posibilidad de accidentes o lesiones.
Efectos del medicamento

Los efectos adversos de la carbinoxamina incluyen somnolencia, depresión del sistema nervioso central, aumento de la presión ocular, agrandamiento de la obstrucción urinaria de la próstata y trastorno de la tiroides.
Esto plantea un riesgo significativo, especialmente para aquellos que padecen trastorno por déficit de atención e hiperactividad (TDAH) y narcolepsia.
Hasta la fecha, Azurity Pharmaceuticals, Inc. no ha recibido informes de eventos adversos graves relacionados con este retiro del mercado.
Sin embargo, la compañía está tomando medidas proactivas para garantizar la seguridad de los pacientes y evitar cualquier posible complicación.
Diferencia del medicamento

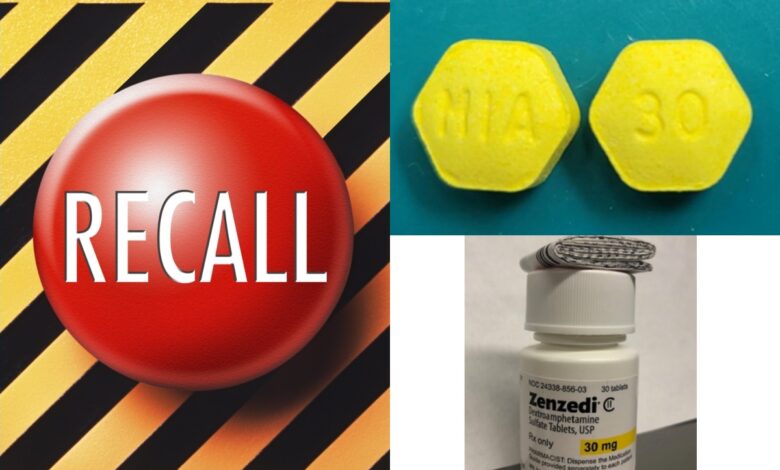
Los comprimidos de Zenzedi® 30 mg afectados se pueden identificar por su forma hexagonal, color amarillo claro, con la inscripción «30» en un lado y «MIA» en el otro.
Se distribuyeron en frascos blancos con escritura negra y «30 mg» resaltado en amarillo.
En contraste, las tabletas incorrectas (carbinoxamina USP, 4 mg) son redondas y blancas, con impresiones de «GL» en un lado y «211» en el otro.
El producto se distribuyó a nivel nacional a través de farmacias.
Medidas contra el error

Azurity Pharmaceuticals, Inc. ha tomado medidas inmediatas para abordar este problema, enviando cartas de notificación de retiro del mercado a distribuidores mayoristas el 4 de enero de 2024.
Además, la compañía ha coordinado la devolución de todos los productos retirados a nivel mayorista.
Además de que está trabajando estrechamente con mayoristas y minoristas para facilitar la recuperación y reemplazo del producto afectado.
La empresa ha contratado los servicios de Inmar Intelligence para gestionar el proceso de retirada.
Qué hacer en caso de tenerlo

Los consumidores que tengan productos afectados deben dejar de usarlos y devolverlos al lugar de compra.
Para obtener información adicional sobre este retiro del mercado, se han proporcionado números de teléfono específicos para consultas relacionadas con el proceso de retirada.
Además de para obtener información médica o técnica sobre el producto.
Siendo Inmar Intelligence al 877-804-2069 (de lunes a viernes, de 9 a. m. a 5 p. m. EST) para el recall y 800-461-7449 (de lunes a viernes, de 9 a. m. a 5 p. m. EST) para información médica.
Información adicional y apoyo

Este retiro del mercado cuenta con el respaldo y conocimiento de la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA).
Se alienta a los consumidores a comunicarse con su médico o proveedor de atención médica si han experimentado algún problema relacionado con el uso de este medicamento.
Además de informar cualquier reacción adversa al programa MedWatch Adverse Event Reporting de la FDA.
Azurity Pharmaceuticals, Inc. reafirma su compromiso con la seguridad de los pacientes y sigue trabajando activamente para abordar esta situación y evitar posibles riesgos para la salud.
 Artículo relacionado
Artículo relacionado




